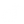 |
Ureyim.az |
Etilenqlikol — ikiatomlu spirtlərin ən sadə nümayəndəsidir. CnH2n(OH)2 (n≥2). Etilenqlikol (CH2OH-CH2OH) (etandiol-1,2) — doymuş ikiatomlu spirtlərin ən sadə nümayəndəsidir. Qlikol sırasının ümumi formulu CnH2n(OH)2-dir. Qlikol adı onlara sıranın bir çox üzvünün şirin olduğu üçün verilmişdir (yunanca qlikos — şirin deməkdir).
| Etilenqlikol | |
|---|---|
 | |
 | |
| Ümumi | |
| Kimyəvi formulu | C₂H₆O₂[1] |
| Molyar kütlə | 0 kq[1] |
| Fiziki xassələri | |
| Sıxlıq | 1,11 ± 0,01 q/sm³[2] |
| Termik xüsusiyyətlər | |
| Ərimə nöqtəsi | 9 ± 0 ℉[2], −13 °C[3][4] |
| Qaynama nöqtəsi | 388 ± 1 ℉[2], 197 °C[5], 197,34 °C[4] |
| Buxarın təzyiqi | 7.900 millipascal[6] |
| Kimyəvi xassələri | |
Turşunun dissosasiya sabiti  |
15,1 ± 0,1[6] |
| Optik xüsusiyyətlər | |
| Sındırma əmsalı | 1,3811[7] |
| Təsnifatı | |
| CAS-da qeyd. nöm. | 107-21-1 |
| PubChem | 174 |
| RTECS | KW2975000 |
| ChEBI | 30742 |
| ChemSpider | 13835235 |
Etilenqlikol etilenin kalium permanqanat və ya digər oksidləşdiricilərlə oksidləşdirilməsindən, yaxud etileni etilenxlorhidrinə çevirib, sonuncunun hidrolizindən alınır. bundan başqa o, doymuş karbohidrogenlərin dihalogenli törəmələrinin qələvi məhlulu ilə qarşılıqlı təsirindən alınır.
Şərbətə bənzər, şirin dada malik, rəngsiz, iysiz, zəhərli mayedir. Etilenqlikol 197,6 ºC-də qaynayır, suda, etanolda yaxşı həll olur. İkiatomlu spirtlərdə həm molekullar arası, həm də molekuldaxili hidrogen rabitəsi var. Hiqroskopikdir.
Etilenqlikolun kimyəvi xassələri əsas etibarı ilə biratomlu spirtlərin xassələrinə uyğun gəlir. Ancaq reaksiyalar həm bir, həm də iki hidroksil qrupları ilə gedir. belə ki, qələvi metallarla etilenqlikol natamam və tam qlikolyatlar əmələ gətirir.
Etilenqlikolun suda və spirtdə məhlulları aşağı temperaturda donmadığından qışda avtomobil və aviasiya motorlarının radiatorlarında antifriz adı ilə işlədilir. Ondan həmçinin qiymətli sintetik lif — lavsan almaq üçün istifadə olunur.
Abbasov V.M., Məhərrəmov M.M., Xanlarov T.N.. Kimya qəbul imtahanına hazırlaşan abituriyentlər üçün dərs vəsaiti.